Yasal Uyarı: Bu sitede yayınlanmakta olan tüm yapıtlar eser statüsünde olup 5846 Sayılı Fikir ve Sanat Eserleri Kanunu ve 5237 sayılı Türk Ceza Kanunu kapsamında korunmaktadır. Sitede bulunan yazı ve görsellerin site sahibinden izin alınmadan ve kaynak gösterilmeden kopyalanması ve kullanılması yasaktır.
Hayır, yanlış okumadınız.
Aşılı çocuklarımızdan aşısız arkadaşlarına nasıl hastalık bulaşı olabileceğini ve hatta olduğunu okuyacaksınız bu sayfada. Hazırsanız buyrun tıp literatüründe kısa bir yolculuğa…
Bir tıp dergisi var, adı Vaccine. Türkçesi ‘Aşı’. 2013’te bu dergide yayımlanmış çığır açıcı çalışmanın başlığı “Zayıflatılmış canlı rotavirüsü aşısı ile pentavalan reassortan* rotavirüsü aşısı sonrasında oluşan ‘virüs dökümü’ karşılaştırması”.
*Reassortan virüs: İnsanda görülen rotavirüsünün aşı geliştirme işlemleri için hücre ortamında kültürlenmesi çok zor olduğundan maymun ve sığırlarda görülen rotavirüsleriyle aynı hücrede kültürleniyor ve bu farklı canlı türlerinden gelen virüsler birbiriyle genetik materyal alışverişine girerek ortaya yeni, hibrid bir virüs çıkıyor.
Çalışmada geçen bilgiler arasında rotavirüsü aşılarında bulunan canlı virüslerin enfeksiyon yapma, dışkı yoluyla çevreye yayılma (shedding/virüs dökme) ve hatta aşısız kişilere bulaşma kabiliyeti yer alıyor. İfade tam olarak şöyle:
“Ve hatta aşılanan kişide hastalık belirtisi olmamasına rağmen bu iki rotavirüs aşısının veya aşıdaki reassortan virüs suşlarının aşısız temaslılara bulaştığı tespit edilmiştir [9 – 13] [1]”.
Bu bilgiyi doğrulamak için kaynak olarak verilen ve aşılıların aşısızları enfekte edebileceğini gösteren beş çalışmadan biri, 2009 yılında yayımlanmış ve rotavirüs aşısı kaynaklı virüsün aşısız temaslılara bulaşarak acil tıbbi müdahale gerektirecek nitelikte semptomatik rotavirüs gastroenteritine neden olduğunu bildirmiş literatürdeki ilk çalışma: “Aşı (RotaTeq) kaynaklı rotavirüsünün kardeşten kardeşe bulaşı ve müteakip rotavirüs *gastroenteriti”.
*Gastroenterit: Mide ve ince bağırsak mukozalarının, kusma, karın ağrısı ve ishal ile belirgin -bazen ateşin de eşlik ettiği- akut iltihabı.
Şöyle diyor çalışmada:
“Burada, aşılanmış bir bebekten aşısız, büyük kardeşe aşı kaynaklı rotavirüs (RotaTeq [Merck and Co, Whitehouse Station, NJ]) bulaşını ve buna bağlı olarak gelişen ve acil servis yatışı gerektiren semptomatik rotavirüs gastroenteritini bildiriyoruz.”
Çalışmada ayrıca RotaTeq aşısındaki 5 virüs suşundan ikisinin ya aşının uygulandığı bebekte ya da daha sonra bulaştığı aşısız kardeşte “reassortasyon”a giderek, yani birbiriyle yeni bir birleşime girerek daha tehlikeli bir virüse dönüşmüş olduğu söyleniyor:
“Yaptığımız incelemeler, aşı virüsü suşlarından P7[5]G1 ve P1A[8]G6 genotipleri arasında ya aşılı bebekteyken ya da kardeşine bulaştığında replikasyon sırasında yeniden birleşim meydana gelmiş olduğunu gösteriyor, bu da yeniden birleşme sonucu ortaya çıkan yeni virüsün aşı virüsünün hastalık yapma gücünü arttırmış olma ihtimalini güçlendiriyor.”
RotaTeq aşısındaki virüs suşları arasındaki bu yeni birleşim oluşturma fenomeni ve aşılılarda buna müteakip ortaya çıkan gastroenterit enfeksiyonu 2012’deki bir araştırmaya göre 61 bebekte daha gözlemlenmiş.[2] Bunun dışında yine 2012 tarihli ve bu defa Nikaragua’dan bir çalışmanın bulgusu şu:
“RotaTeq aşısının yaygın kullanımı, aşıdaki virüs genlerinin dolaşımdaki insan Rota virüslerine karışmasına yol açmıştır.”
Yani, yoğun aşılama nedeniyle bugün yakalandığımız (doğadaki) vahşi virüsün genetik yapısını değiştirmiş bulunuyoruz. [3]
Tahminler, aşılanan bebeklerin %80 ila %100’ünün aşılamayı takip eden 25 ila 28 gün içinde, bir noktada rotavirüsünü vücuttan dışarı attığı [shedding] yönünde.[4] [5] Bu durumda, aşısız çocuklarla ilgili bizlere aşılanmaya çalışılan genel kanının aksine, bizzat aşılı çocukların aşısızlara hastalık bulaştırma riski bariz şekilde ortada ve hatta düşünecek olursak, aşılarda kullanılan farklı türden rotavirüslerinin bu çocukların bedeninde rekombinasyon yoluyla değişime uğrayıp, aşının etki bile etmeyeceği yeni “süper virüsler”e dönüşmesi için ideal virolojik koşulları da sağlıyor bu aşılı çocuklar.
National Vaccine Information Center’ın bulduğu bir başka aşı kaynaklı virüs dökme (shedding) olgusu:
“2010’da Pediatrics dergisinde yayımlanan bir olgu sunumunda hiç rota aşısı almamış olmasına rağmen aşı tipi rotavirüsü ile enfekte 30 aylık sağlıklı erkek çocuk tanımlanıyor. 237 Bu çocuk, 2 aylık sağlıklı erkek kardeşi Merck’ün RotaTeq aşısını olduktan 10 gün sonra ağır gastroenterit tanısı ile acil servise kaldırılıyor. Acilde alınan dışkı numunesi RT-PCR testi ile analiz edildiğinde RotaTeq aşısında kullanılan tipte virüs tespit ediliyor.”
Olgu sunumunun yazarları “ruhsatlandırma öncesi klinik deneylerde RotaTeq aşısındaki viral suşların aşısız temaslılara bulaşma riskinin çalışılmamış olduğu” notunu düşüyor. Hem RotaTeq hem de [GlaxoSmithKline Biologicals’a ait] Rotarix‘in “temaslılara aşı virüsü bulaştırma potansiyeli olduğu”nu da ekliyorlar.
RotaTeq aşısı: Cerahat Toplamış Buz Dağının Görünen Kısmı
RotaTeq marka rotavirüs aşısının yaratıcılarından biri Dr. Paul Offit biliyoruz. Kendisini aşı endüstrisinin bir numaralı destekçisi ve apolojisti olarak tanıyoruz. Amerikan Gıda ve İlaç Dairesi FDA’nın onay verdiği ve CDC’nin de Amerika’da bebeklere 2., 4. ve 6. aylarda 3’er doz uygulanmak üzere önerdiği iki canlı rotavirüsü aşısından birinin patent ortağı aynı zamanda.
Endüstri ile menfaat ilişkisi daha bariz olamayacak bu hekimin usulen, tarafsız olmadığı için karar alıcı mekanizmada söz sahibi olmaktan imtina etmesi gerekirken, yaptığı açıklamalarda aşısını ve elbette CDC’nin genel aşı takvimini “etkili ve güvenli” ilan etmesi elbette şahsi maddi kazanç elde etmesine yarayacak bu hekim kendisini her fırsatta aşı uzmanı olarak ortaya koyuyor ve söz alıyor. Örneğin, Parenting adlı dergide yayımlanan bir röportajında çocukların hiç sorunsuz aynı anda 10,000 aşı birden olabileceği ifadesi hayli meşhurdur Offit’in, kaldı ki bu 10,000 sayısı da aslında daha önce bir başka röportajda dillendirdiği 100,000’e gelen tepkiler üzerine düzeltme yaptığı halidir.
Age of Autism adlı otizm konusunda yayın yapan sitede yer verilen karnesine bakıyoruz Dr. Offit’in:
- Merck şirketinden çıkan Rotavirüs aşısının patent sahibi Paul Offit, Amerika’da ‘Bağışıklama Uygulamaları Danışma Kurulu’na atanıyor.
- Bu kuruldayken Rotavirüs aşısının ulusal takvime alınması yönünde oy kullanıyor (sözkonusu aşı Merck’ünki değil, zira kendi aşısı henüz piyasaya sürülmeye hazır değil).
- Takvime bu şekilde alınan Rotavirüsü aşısı yarattığı ağır yan etkiler nedeniyle piyasadan çekilmek zorunda kalıyor, ancak bu piyasadan çekme kararının alındığı toplantıda Offit geri çekilsin yönünde oy kullanmayarak çekimser kalmayı tercih ediyor.
- Aradan birkaç yıl geçtikten sonra rotavirüs aşısı yeniden takvimde yerini alıyor, bu defa Offit’in aşısı şeklinde.
- Dr. Offit rotavirüs aşısının patent hakkını Merck’e satarak on milyonlarca doların sahibi oluyor.
En başından kirli aşı – Rotavirüs
Piyasaya ilk çıkan rotavirüs aşısı Rotashield‘da Hint şebeği (Rhesus maymunu) ve insan rotavirüslerinin yeniden birleşiminden oluşan dört virüs tipi bulunuyor. 1999’da onay alıyor bu aşı ve fakat sadece 9  ay içinde bazı çocuklarda bağırsak dönmesi veya düğümlenmesi olarak da bilinen ve ölümcül olabilen ‘intussusception’ vakalarına yol açması [6] nedeniyle FDA tarafından geri çekilmek zorunda kalınıyor.
ay içinde bazı çocuklarda bağırsak dönmesi veya düğümlenmesi olarak da bilinen ve ölümcül olabilen ‘intussusception’ vakalarına yol açması [6] nedeniyle FDA tarafından geri çekilmek zorunda kalınıyor.
Offit’in insan ve sığır retrovirüsü kırması (evet, yani genetiği ile oynanmış) 5 yeni virüsten oluşan Rotateq’i FDA tarafından 2006’da eski aşıya göre daha güvenli olduğu düşünülerek ruhsatlandırılıyor. Ancak araştırmalar bu aşının da eskisiyle aynı ölümcül sorunlara sahip olduğunu gösteriyor.
Vaccine dergisinde 2015 Şubat’ında çıkan “RotaTeq aşılaması sonrasında ortaya çıkan bağırsak düğümlenmesi riski: Olgu sunumu dizileri halinde dünya genelinde yapılmış spontan bildirimler üzerinden değerlendirme” adlı çalışmanın yazarları, “under-reporting” denilen ve gerçekte görülen yan etkilerin çok az kısmının bildirilmesi fenomenini de hesaba katarak RotaTeq’in üreticisine 2014 mayısına kadar tüm dünyadan yapılan yan etki bildirimlerini inceliyor. Çalışmaya göre RotaTeq uygulamasına bağlı ‘bağırsak düğümlenmesi’ riski “aşılamadan sonraki 3 ila 7 gün içinde, özellikle ilk doz sonrasında artış gösteriyor, ikinci ve üçüncü doz alımından sonra ise daha az vaka görülüyor”. Aşının ilk dozundan sonraki 3 ila 7 gün içinde bağırsak düğümlenmesi yaşanma riski aşıdan 15 ila 30 gün sonrasına göre 3.45 kat fazla bulunuyor.
RotaTeq’i bağırsak düğümlenmesi ile ilişkilendiren bir başka çalışma da 2013’te New England Journal of Medicine dergisinde yayımlanmış ve ilk dozu alan her 100,000 çocukta yaklaşık 1.5 ekstradan bağırsak düğümlenmesi vakası oluştuğu saptanmış. [7]
Canlı aşılar: Pandora’nın dışkökenli- virüs-kaynayan kutusu
RotaTeq aşısını takiben ölüm veya bağırsaklarda kişiyi perişan eden tıkanma tıbben kaçırılması mümkün olmayan akut aşı reaksiyonları. Aşıların piyasaya çıkış sonrası yan etkilerini izlemek amacıyla oluşturulmuş pasif, yani bildirim mecburiyeti bile olmayan Aşı Sonrası İstenmeyen Etki (ASİE) Bildirim Sistemi’nde RotaTeq’e bağlı bu sorunların ‘önemli yan etki’ olarak belirmesi bu yüzden daha da dikkat çekici. ABD’deki ASİE sisteminin aşı sonrası oluşan gerçek yan etkilerin %1’inden de azını ihtiva ettiği FDA ve CDC tarafından da dile getirildiğine göre, RotaTeq’in verdiği gerçek zararın bu raporda gözükenin onlarca kat fazlası olduğu açık.
RotaTeq alımına bağlı istenmeyen etkilerin, diğer pekçok canlı virüs aşısı için de geçerli olduğu gibi, bu saydıklarımızdan da karanlık bir tarafı daha var. Modern yaşamda maruz kaldığımız toksisitelerinin multifaktöryel sis bulutlarının parçası olarak belki aylar, belki yıllar ve belki de onyıllar sonra kendini belli edecek ve yolun sonunda klasik bir teşhisle taçlandırılacak etkiler bunlar.
RotaTeq aşısında örneğin bugüne kadar çok sayıda dış kaynaklı virüs kontaminasyonu tespit edilmiş durumda. Aşı ilk üretilmeye çalışıldığı sırada kullanılan canlı hücrelerde ve/ya aşının diğer biyolojik bileşenlerinde ta o zamandan çeşitli virüslerin olması anlamına geliyor bu. Mevcudiyeti aşı üreticisinin de, aşıyı onaylayan kurumun da gözünden kaçan, üretildiği sırada varlığı dahi bilinmeyen bu ajanlar maalesef çocuklara verilen aşıları enfekte etmiş durumda.
Bugüne kadar hangi yabancı virüsler mi bulunmuş RotaTeq’te:
Porcine Circovirus 1 (PCV-1): Domuz Sirkovirüsü Tip 1 (Porsin Sirkovirüs Tip 1)
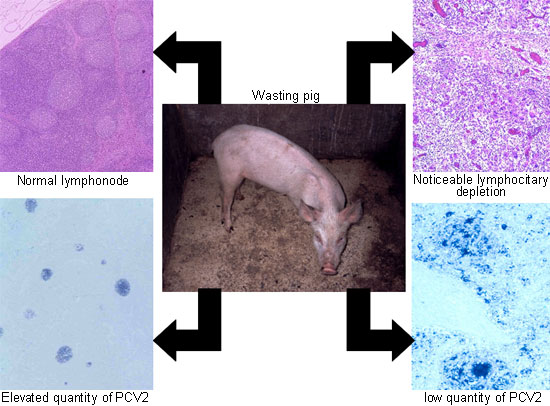
2010 yılında FDA, Rotarix aşısına bu insanlardaki etkisi hala bilinmeyen domuz virüsünün (PCV-1’in) karışmış olduğu tespit edilir edilmez uygulamayı askıya alıyor. Yaptığı incelemeler sonrası FDA, domuz yavrularında “wasting” denilen erime sendromuna yol açan PCV-2’ye göre daha az riskli olduğu kabul edilen bu 1. tip sirkovirüsün uygulandığı milyonlarca çocuk için risk teşkil etmeyeceğine hükmediyor.
Porcine Circovirus 2 (PCV-2): Domuz Sirkovirüsü Tip 2 (Porsin Sirkovirüs Tip 2)
2014’te CDC’de görevli araştırmacıların yürüttüğü ve Human Vaccines & Immunotherapeutcs (İnsan Aşıları ve İmmünoterapötikleri) adlı dergide yayımlanan “RotaTeq® ile aşılanmış bebeklere ait dışkı numunelerinde PCV-2 DNA’sı tespiti” başlıklı çalışma ile ilk defa bu aşıyı almış çocukların PCV-2 virüsünü dışkıdan attıkları tespit edilmiş oluyor.
Aşılanmış 59 çocuktan aldıkları kaka numunelerinin 235’inde (yani %28.5’inde) PCV-2 DNA’sı bulunuyor. Ek olarak, “102 aşılının 22’sinin (%21.6’sının) RotaTeq® aşı virüsünü kakayla attığı ve 10’unun da (%9.8) hem PCV DNA’sı hem de aşı tipi rotavirüsü RNA’sını kaka yoluyla vücuttan attığı” tespit ediliyor.
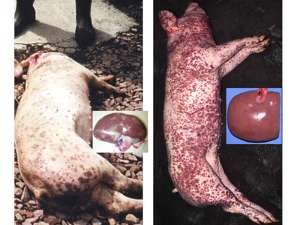
Domuzlarda PCV-2 enfeksiyonunun yol açtığı ciddi sağlık sorunları şunlar:
PCV-2’e bağlı zatürre, PCV-2’ye bağlı enterit (bağırsak iltihabı), PCV-2’ye bağlı üreme sistemi sorunları ve Porsin Dermatiti ve Nefropati Sendromu (Domuzlarda Deri İltihabı ve Böbrek Hastalığı Sendromu). [kaynak]
2010’da FDA tıpta ihtiyat prensibini çiğneyerek, “PCV2 domuzlarda hastalığa yol açabiliyor olsa da ne PCV1 ne de PCV2’nin insanda enfeksiyona veya hastalığa yol açtığına dair kanıt olmadığı” yönünde karar alıyor.
7 numaralı endojenöz Babun maymunu retrovirüsüne ait DNA: Advances in Virology dergisinde 2014’te yayımlanmış çalışmanın başlığı “Aşılama sonrası pediyatrik ileal doku numunelerinde viral patojen taraması.” Sonuç, babunlarda görülen bir retrovirüsle kontaminasyon.
D Sınıfı Maymun Retrovirüsü: Journal of Virology‘de 2010’da yayımlanan bir çalışmayla da RotaTeq aşısında (eşleşme kesinliği %96 çıkan) maymun retrovirüsü DNA’sı olduğunu öğreniyoruz. Mikrobiyolog Judy Mikovits, bu retrovirüsün kendi kendine çoğalıp çoğalamamasından (replikasyon kabiliyetinden) bağımsız olarak, tuttuğu konağın sağlığına olumsuz etki edebileceğini teyit ediyor.
Canlı virüs aşıları üretilirken farklı canlı türlerinden hücre ve biyolojik sıvılar birarada kültürlendiğinden, ihtiva ettikleri virüslerin birbirine adapte olup, yeni birleşimlere girerek aslından çok daha virülan, yani hastalık yapma etkisi çok daha kuvvetli enfeksiyöz ajanlara dönüşmeleri için fazlasıyla imkanları var.
RotaTeq, ulusal aşı takvimlerinde yerini almış ve taşıdıkları retrovirüsler de dahil olmak üzere içeriğindeki canlı virüsler ile aşıyı olan kişiyi bizzat enfekte edebilecek özellikteki onlarca aşıdan yalnızca biri. İşte bu yüzden, modern çağın vebası, insanları enfekte etme kabiliyeti olan bu ‘HIV dışındaki immünyetmezlik virüsleri’ diyor Mikovits. HIV, bildiğimiz gibi ‘insan immünyetmezlik virüsü’ olarak bilinen ve taşıyıcıların %1 ila 5’inde AIDS’e yol açan bir retrovirüs çeşidi. Yavaş yavaş ortaya çıkan gerçekler, bugün laboratuvarlarda aşı veya diğer biyolojik ürünlerin üretim çalışmaları esnasında, kullanılan çeşitli türden canlı dokularındaki endojen retrovirüslerin kontrolsüz şekilde birleşerek ortaya yeni ve enfeksiyon kabiliyeti olan retrovirüsler çıkardığını ve mevcut teknolojiyle bu yeni oluşumlu retrovirüslerin tamamının tespit edilmesinin imkansız olduğunu gösteriyor. Bu konuyla ilgili ayrıntılı bilgi için Dr. Judy Mikovits ve Kent Heckenlively’nin kaleme aldığı Plague adlı kitabı okuyabilirsiniz.
RotaTeq aşısının taşıdığı potansiyel olumsuz etkiler bu şekilde açıkça ortadayken, özellikle de bu aşıyı olanların aşıya karışmış virüslerle enfekte olma ihtimalleri sözkonusuyken, tıpta ihtiyat prensibi gereğince ilgili toksikolojik değerlendirmeler yeniden yapılıncaya dek aşılamanın askıya alınması icap eder. Amerika Birleşik Devletleri’nden tüm dünyaya ihracını gördüğümüz mevcut aşılama takviminin güvenli olup olmadığını sorgulayan herkes ilk başta bu RotaTeq aşısını göstererek bağışıklama uygulamalarının neden “kanıta dayalı” olmadığını, aksine hiçbir şekilde ne güvenliği ne de etkinliği kanıtlanmış bu ürünlerin mitolojik bir inanç sarmalında bizlere hayat kurtaran mucize ilaçlar olarak sunulduğunu ifade edebilir.
Bu yazı için GreenMedinfo’nun makalesinden yararlanılmıştır.
Kaynaklar:
[1] [9] Phua KB, Quak SH, Lee BW, Emmanuel SC, Goh P, Han HH, et al. Evaluation of RIX4414, a live, attenuated rotavirus vaccine, in a randomized, double-blind, placebo-controlled phase 2 trial involving 2464 Singaporean infants. J Infect Dis 2005;192(Suppl. 1):S6 – 16. [2] J Infect Dis. 2012 Aug 1;206(3):377-83. doi: 10.1093/infdis/jis361. Epub 2012 May 21.Identification of strains of RotaTeq rotavirus vaccine in infants with gastroenteritis following routine vaccination. Donato CM1, Ch’ng LS, Boniface KF, Crawford NW, Buttery JP, Lyon M, Bishop RF, Kirkwood CD.
[3] Infect Genet Evol. 2012 Aug;12(6):1282-94. doi: 10.1016/j.meegid.2012.03.007. Epub 2012 Apr 2.Vaccine-derived NSP2 segment in rotaviruses from vaccinated children with gastroenteritis in Nicaragua. Bucardo F1, Rippinger CM, Svensson L,Patton JT.
[4] Phua KB, Quak SH, Lee BW, Emmanuel SC, Goh P, Han HH, et al. Evaluation ofRIX4414, a live, attenuated rotavirus vaccine, in a randomized, double-blind, placebo-controlled phase 2 trial involving 2464 Singaporean infants. J Infect Dis 2005;192(Suppl. 1):S6 – 16.
[5] Comparison of virus shedding after lived attenuated and pentavalent reassortant rotavirus vaccine [6] Centers for Disease Control and Prevention. Intussusception among recipients of rotavirus vaccine – United States, 1998 – 1999. JAMA 1999;282:520-1CrossRefMedlineWeb of Science [7] N Engl J Med. 2014 Feb 6;370(6):503-12. doi: 10.1056/NEJMoa1303164. Epub 2014 Jan 14 Intussusception risk after rotavirus vaccination in U.S. infants. Yih WK1, Lieu TA, Kulldorff M, Martin D, McMahill-Walraven CN, Platt R, Selvam N, Selvan M, Lee GM, Nguyen M [10] Dennehy PH, Brady RC, Halperin SA, Ward RL, Alvey JC, Fischer Jr FH, et al. Comparative evaluation of safety and immunogenicity of two dosages of an oral live attenuated human rotavirus vaccine. Pediatr Infect Dis J 2005;24:481 – 8. [11] Payne DC, Edwards KM, Bowen MD, Keckley E, Peters J, Esona MD, et al. Sibling transmission of vaccine-derived rotavirus (RotaTeq) associated with rotavirus gastroenteritis. Pediatrics 2010;125:e438 – 41. [12] Boom JA, Sahni LC, Payne DC, Gautam R, Lyde F, Mijatovic-Rustempasic S, et al. Symptomatic infection and detection of vaccine and vaccine-reassortant rotavirus strains in 5 children: a case series. J Infect Dis 2012;206:1275 – 9. [13] RiveraL,Pen ̃aLM,StainierI,GillardP,CheuvartB,SmolenovI,etal.Horizontal transmission of a human rotavirus vaccine strain – a randomized, placebo- controlled study in twins. Vaccine 2011;29:9508 – 13.Yasal Uyarı: Bu sitede yayınlanmakta olan tüm yapıtlar eser statüsünde olup 5846 Sayılı Fikir ve Sanat Eserleri Kanunu ve 5237 sayılı Türk Ceza Kanunu kapsamında korunmaktadır. Sitede bulunan yazı ve görsellerin site sahibinden izin alınmadan ve kaynak gösterilmeden kopyalanması ve kullanılması yasaktır.







Geri İzlemeler/Pingbackler